- Autor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:49.
- Naposledy zmenené 2025-06-01 07:37.
Kľúčový rozdiel medzi oxidom dusnatým a oxidom dusnatým je ten, že oxid dusnatý je bezfarebný plyn, zatiaľ čo oxid dusnatý je biela pevná látka.
Oxid dusnatý a oxid dusnatý sú chemické zlúčeniny obsahujúce dusík a kyslík. Sú to oxidy dusíka. Majú však odlišné chemické a fyzikálne vlastnosti.
Čo je oxid dusnatý?
Oxid dusnatý je anorganická zlúčenina s chemickým vzorcom NO. Nazývame ho oxid dusnatý, pretože je to oxid dusíka. Je to vlastne voľný radikál, pretože má nepárový elektrón. Navyše je to heteronukleárna dvojatómová molekula.
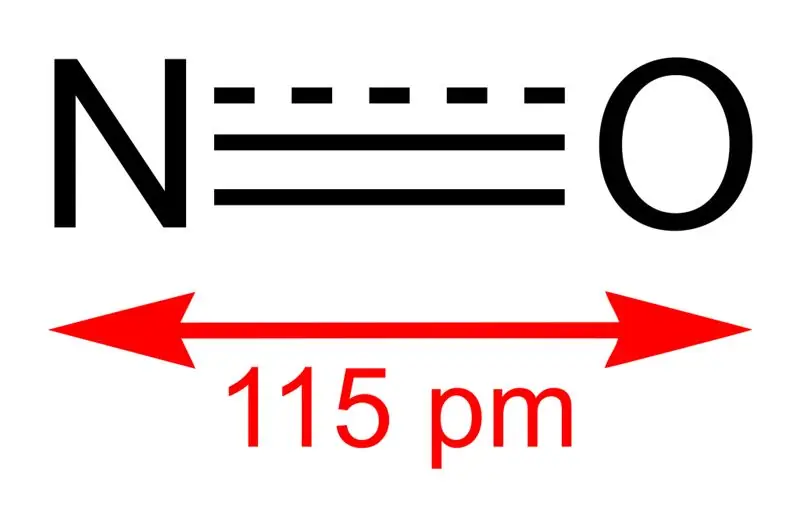
Obrázok 01: Štruktúra oxidu dusnatého a dĺžka väzby medzi N a O
Molárna hmotnosť tejto zlúčeniny je 30 g/mol. Vyskytuje sa ako bezfarebný plyn. Okrem toho, jeho bod topenia je -164 °C, zatiaľ čo bod varu je -152 °C, čo sú veľmi malé hodnoty v porovnaní s hodnotami iných oxidov dusíka. Tento voľný radikál môžeme vyrobiť oxidáciou amoniaku pri 850 °C v prítomnosti platinového katalyzátora. V laboratórnom meradle ho však vieme pripraviť redukciou zriedenej kyseliny dusičnej meďou.
Čo je oxid dusný?
Oxid dusný je anorganická zlúčenina s chemickým vzorcom N2O5 Nazývame ho oxid dusnatý. Je to binárny oxid dusíka. Navyše je nestabilný a môže pôsobiť ako nebezpečné oxidačné činidlo. Molárna hmotnosť zlúčeniny je 108,01 g/mol. Vyskytuje sa ako biela pevná látka.
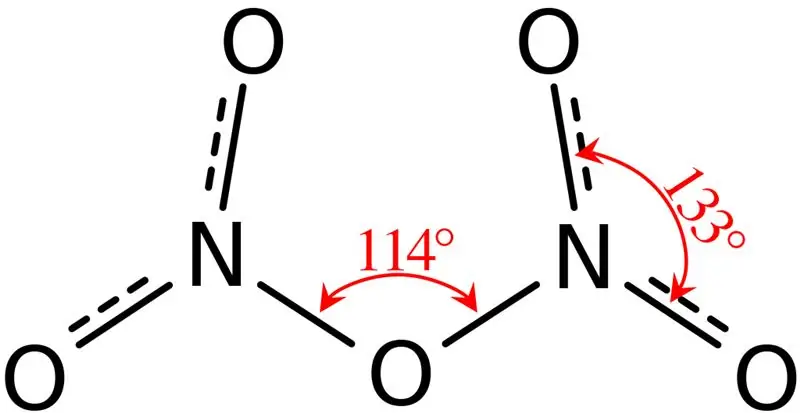
Obrázok 02: Štruktúra oxidu dusného
Navyše, bod topenia tejto zlúčeniny je 41 °C a pri 47 °C táto zlúčenina podlieha sublimácii. Táto zlúčenina reaguje s vodou za vzniku kyseliny dusičnej. Navyše, molekulárny tvar molekuly oxidu dusného je rovinný. Túto zlúčeninu môžeme vyrobiť dehydratáciou kyseliny dusičnej s oxidom fosforečným.
Aký je rozdiel medzi oxidom dusnatým a oxidom dusnatým?
Oxid dusnatý je anorganická zlúčenina s chemickým vzorcom NO, zatiaľ čo oxid dusnatý je anorganická zlúčenina s chemickým vzorcom N2O5 Kľúčový rozdiel medzi oxidom dusnatým a oxidom dusnatým je v tom, že oxid dusnatý je bezfarebný plyn, zatiaľ čo oxid dusnatý je biela pevná látka. Okrem toho vieme vyrobiť oxid dusnatý oxidáciou amoniaku pri 850 °C v prítomnosti platinového katalyzátora. Výroba oxidu dusného sa však uskutočňuje dehydratáciou kyseliny dusičnej oxidom fosforečným. Pri zvažovaní tvaru molekuly je oxid dusnatý lineárny, zatiaľ čo oxid dusnatý je rovinný.
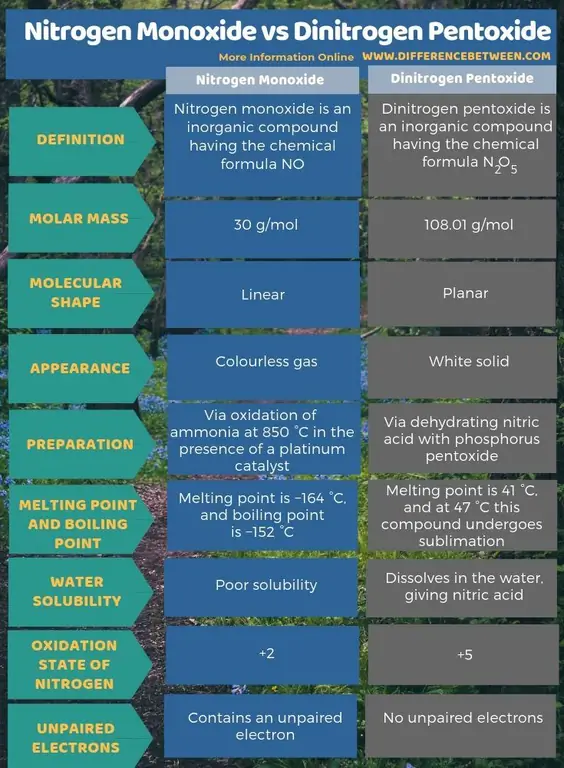
Zhrnutie - oxid dusnatý vs oxid dusný
Oxid dusnatý je anorganická zlúčenina s chemickým vzorcom NO, zatiaľ čo oxid dusnatý je anorganická zlúčenina s chemickým vzorcom N2O5 Kľúčový rozdiel medzi oxidom dusnatým a oxidom dusnatým je v tom, že oxid dusnatý je bezfarebný plyn, zatiaľ čo oxid dusnatý je biela pevná látka.






